Introducción y fundamentos de bioquímica
(Jesús Díaz, 24 Septiembre 2020)
Enlaces complementarios:
Química General, Biología molecular, Genética, Espectroscopia Molecular, Método Científico
Nota de voz
Prólogo
El objetivo de la ciencia de la bioquímica es explicar la vida en términos moleculares.
¿Qué es la vida?¿Qué es lo que distingue a la materia viva de la que no tiene vida?
La vida es un fenómeno de la segunda generación de estrellas. Esta afirmación, basada en el hecho empírico que domina a toda ciencia, se basa en el hecho de que la vida, tal como la concebimos, sólo pudo aparecer cuando eran abundantes determinados elementos químicos como carbono, hidrógeno, oxígeno, nitrógeno y fósforo (C, H, O, N y P).
La cualidad principal que diferencia a la vida es la constante renovación de una estructura muy ordenada, que se acompaña a menudo de un aumento de la complejidad de esa estructura. La vida se basa en la creación y duplicación de orden en un medio caótico. Esta ordenación utiliza energía.
Los organismos crean un orden molecular magnífico dentro de ellos mismos y transmiten un patrón de ese orden a sus descendientes. Esta creación y duplicación del orden, que se diferencia del entorno a menudo caótico, es una característica propia de la vida, y parece ir en contra de una de las leyes fundamentales del universo, la segunda ley de la termodinámica.
Una forma de expresar esta segunda ley es la siguiente: el desorden global del universo aumenta de manera continua. Pero la segunda ley de la termodinámica no exige que el desorden aumente en todos los lugares y en todos los momentos; las criaturas vivas son como pequeños remolinos de orden dentro de la corriente del universo.
No obstante, las leyes de la termodinámica exigen que esta creación local de orden y complejidad en la materia esté compensada por un gasto continuo de energía. Éste es el motivo por el que los seres vivos deben captar siempre energía de su entorno, ya sea de la luz solar, como hacen las plantas, ya sea del alimento, como hacen los animales.
Las criaturas vivas de la tierra están formadas fundamentalmente por muy pocos elementos; básicamente, carbono, hidrógeno, oxígeno y nitrógeno (C, H, O, N). Adviértase que estos elementos, con la adición del helio y el neón, son también los más abundantes del universo.
La abundancia de oxígeno e hidrógeno en los organismos se explica en parte por el importante cometido que desempeña el agua en la vida sobre la tierra.
Los elementos C, H, O y N son importantes para la vida, debido a su fuerte tendencia a formar enlaces covalentes. En concreto, la estabilidad de los enlaces carbono-carbono y la posibilidad de formar enlaces simples, dobles o triples dan al carbono la versatilidad necesaria para formar parte de una enorme diversidad de compuestos químicos.
Un “segundo nivel” de elementos esenciales es el formado por el azufre y el fósforo, que forman enlaces covalentes, y los iones Na1-, K+, Mg2+, Ca2+ y Cl_. El azufre es un componente importante de las proteínas, y el fósforo desempeña funciones esenciales en el metabolismo energético y en la estructura de los ácidos nucleicos.
La mayor parte de estos elementos de tercer y cuarto nivel son metales, y algunos de ellos actúan como colaboradores de la catálisis de las reacciones bioquímicas.
Actualmente está bien establecido que la materia viva cumple las mismas leyes físicas fundamentales que gobiernan a toda la materia. En consecuencia, es posible aplicar toda la potencia de las modernas teorías químicas y físicas a los problemas biológicos.
Para comprender cualquier proceso vital es necesario, pues, comprender su química.
La comprensión de la base molecular de la vida. La interacción creciente de la medicina. Las discusiones de las enfermedades moleculares, tales como la anemia falciforme, y de los mecanismos de acción de fármacos, como la penicilina, enriquecen la enseñanza de la bioquímica. En investigación áreas tales como la base molecular de la excitabilidad.
¿Cuál preparación y nivel necesitamos para iniciar de forma convencional este estudio de la bioquímica?
Para comprender la bioquímica, es preciso estudiar antes la química general, estequiometría, reacciones y los principios básicos de la termodinámica de la física.
Introducción
Antonie van Leeuwenhoek (1632-1723) fue un comerciante de telas holandés aficionado a tallar lentes, el padre de la microbiología, por sus excepcionales observaciones del mundo microbiano a través de unos sencillos microscopios que él mismo se construía. Leeuwenhoek fue la primera persona que vio bacterias.
La palabra «célula» fue usada por primera vez en sentido biológico por el científico inglés Robert Hooke (1635-1701).
La bioquímica, anteriormente llamada de química biológica o fisiológica, surgió a partir de las investigaciones de fisiologistas y químicos sobre compuestos y reacciones químicas en seres humanos y plantas el siglo XIX.
La química de la vida ya estaba establecida como ciencia, bajo diferentes denominaciones. Entre los momentos más importantes de la historia de la bioquímica, se destacan:
- Friedrich Wöhler, en 1828 publicó un artículo acerca de la síntesis de urea, probando que los compuestos orgánicos pueden ser creados artificialmente, en contraste con la creencia, comúnmente aceptada durante mucho tiempo, que la generación de estos compuestos era posible sólo en el interior de los seres vivos.
- Anselme Payen, en 1893 descubrió la primera enzima, la diastasa.
Desde entonces, la bioquímica ha avanzado, especialmente desde la mitad del siglo XX con el desarrollo de nuevas técnicas como la cromatografía, la difracción de rayos X, marcaje por isótopos y el microscopio electrónico. Estas técnicas abrieron el camino para el análisis detallado y el descubrimiento de muchas moléculas y rutas metabólicas de las células, como la glucólisis y el Ciclo de Krebs (denominado así en honor al bioquímico Hans Adolf Krebs).
Uno de los avances más importantes se produjo en 1953 cuando Watson y Crick describieron la estructura de doble hélice del DNA gracias a los resultados obtenidos por Rosalind Franklin.
Durante principios de la década de 1900-1909 el médico inglés Archibald Garrod estudió a pacientes que tenían los trastornos relativamente raros de alcaptonuria, albinismo, cistinuria y pentosuria, además de que estableció que dichas enfermedades estaban determinadas genéticamente. Garrod designó a estas enfermedades errores congénitos del metabolismo; sus ideas constituyeron los cimientos para el desarrollo del campo de la genética bioquímica humana.

El conocimiento de los temas bioquímicos listados por arriba de la línea verde del diagrama ha aclarado el entendimiento de las enfermedades mostradas por debajo de dicha línea. A su vez, los análisis de las enfermedades han aclarado muchas áreas de la bioquímica.
Note que la anemia de células falciformes es una enfermedad genética y que tanto la aterosclerosis como la diabetes mellitus tienen componentes genéticos.
La mayoría de las enfermedades tienen una base bioquímica
Además de microorganismos infecciosos y contaminantes ambientales, muchas enfermedades son manifestaciones de anormalidades en genes, proteínas, reacciones químicas, o procesos bioquímicos, cada uno de los cuales puede tener efectos adversos sobre una o más funciones bioquímicas cruciales.
Los ejemplos de las alteraciones de la bioquímica del ser humano de las cuales dependen enfermedades u otros estados debilitantes son desequilibrio de electrólitos, ingestión o absorción defectuosa de nutrientes, desequilibrios hormonales, sustancias químicas o agentes biológicos tóxicos, así como trastornos genéticos basados en el DNA.
Para hacer frente a estos retos, la investigación bioquímica sigue estando entrelazada con estudios en disciplinas como genética, biología celular, inmunología, nutrición, patología y farmacología.
Además, muchos bioquímicos están vitalmente interesados en contribuir a soluciones para problemas clave, como la supervivencia final del género humano, y la educación del público para apoyar el uso del método científico en la resolución de problemas ambientales y otros problemas importantes a los cuales se enfrenta el humano.
composición de los seres vivos
- Solamente unos 30 elementos químicos, de los más de 90 presentes en la naturaleza son, esenciales para los seres vivos.
- La mayoría tienen un número atómico bajo, por debajo de 34.
- Los más abundantes son: H, O, C, N (estos cuatro constituyen más del 95% de la masa celular), p, s, na, k, cl (3% de la masa celular).
- Oligoelementos: fe, mn, mg, zn, mo, se, etc. (> 0,01% de la biomasa). Imprescindibles para la actividad de ciertas proteínas.
Biomoléculas
- La mayoría son compuestos orgánicos (esqueleto carbonado).
- Los C pueden formar cadenas lineales, ramificadas y circulares.
- Al esqueleto carbonado se le añaden grupos de otros átomos, llamados grupos funcionales.
- Las propiedades químicas vienen determinadas por los grupos funcionales.
La unidad de la organización biológica: La célula
Matthias Jacob Schleiden
Biólogo alemán, profesor de la Universidad de Jena. Es uno de los fundadores de la teoría celular (Célula); investigó la unidad de la estructura y del crecimiento de los organismos.
Theodor Schwann
Biólogo alemán, profesor de las Universidades de Lovaina y Lieja (Bélgica), uno de los fundadores de la teoría celular (Célula). Su principal trabajo fue Investigaciones microscópicas sobre la correspondencia en la estructura y crecimiento de los animales y plantas (1839). Las concepciones filosóficas de Schwann poseían elementos de deísmo y de teleología.
Rudolf Carl Virchow
Publicó el Manual de Patología Especial y Terapéutica en seis volúmenes. Uno de sus trabajos más importantes fue el desarrollo de la Teoría celular en la cual postulaba que “toda célula proviene de otra célula”. Este concepto se basó en aportes anteriores de médicos zoólogos y botánicos. Gracias a su trabajo, contribuyó a aumentar en Alemania el número de cátedras de Patología, de dos a dieciocho, y en Austria de una a diez.
Podemos definir la célula como la entidad física que constituye la unidad morfológica y funcional fundamental de la estructura viviente de los organismos.
Estructura de una célula en general
La estructura está formada por la membrana plasmática, envoltura nuclear, material genético y el citoplasma.
Estructura de una célula animal

Tipos de células
Las principales diferencias entre las estructuras celulares definen las dos grandes clases de organismos: procariotas y eucariotas.
Procarióticas
Se caracterizan por carecer de membrana alrededor del núcleo por ello su material genético se encuentra disperso en el citoplasma. (Carecen de los orgánulos con membranas que son característicos de las células eucariotas). Sólo tienen un cromosoma y su citoplasma carece de orgánulos limitados por membrana. Por ejemplo: bacterias y micoplasmas. Las células procariotas no están compartimentadas. Los procariotas, que son siempre unicelulares, comprenden las bacterias verdaderas (eubacterias) y una clase antigua denominada arqueobacterias.
En los procariotas, el citoplasma no está dividido en compartimientos y la información genética se encuentra en forma de una o varias moléculas de DNA que están libres en el citosol. También están suspendidos en el citosol los ribosomas, que constituyen la maquinaria molecular para la síntesis de proteínas. La superficie de las células procariotas puede poseer pili o vellosidades, que facilitan la fijación del organismo a otras células o superficies, y flagelos, que le permiten nadar.
Eucarióticas
Su estructura se compone por: la membrana plasmática, el citoplasma y el núcleo.
Poseen membrana nuclear y presentan orgánulos citoplasmáticos rodeados de membrana. Son más grandes y complejas que las procarióticas. Por ejemplo: hongos, algas, plantas y animales. Las células eucariotas poseen orgánulos limitados por membranas.
Los orgánulos más importantes que son comunes a la mayor parte de las células eucariotas son las mitocondrias, que se especializan en el metabolismo oxidativo; el retículo endoplásmico que es una estructura de membranas plegadas, con abundantes ribosomas y donde tiene lugar gran parte de la síntesis de proteínas; el complejo de Golgi, que son cámaras unidas a membranas que intervienen en la secreción y el desplazamiento intracelular de las nuevas proteínas, y el núcleo.
El núcleo de una célula eucariota contiene la información genética de la célula, codificada en el DNA, que está empaquetado en los cromosomas. Una parte de este DNA está subempaquetado en una región densa del interior del núcleo, denominada nucléolo. Alrededor del núcleo hay una envoltura nuclear, perforada por poros a través de los cuales se comunican el núcleo y el citoplasma.
Estructura de la célula eucariótica
Membrana plasmática
Constituye el límite exterior de la célula. Está compuesta aproximadamente por un 40 % de moléculas de lípidos, 55 % de proteínas y un 5 % de hidratos de carbono. Observando la membrana por el microscopio electrónico aparece una estructura, denominada unidad de membrana, representada por dos bandas oscuras separadas por una clara. Su función más importante es la de proteger la célula y regular la entrada y salida de moléculas.
Citoplasma
Es la parte de la célula comprendida entre la membrana celular y el núcleo. En él se realizan todas las reacciones bioquímicas características de los seres vivos. Está compuesto de:
- A. Citosol o Hialoplasma.
Es una sustancia líquida formada por agua y distintas sustancias disueltas en ella( sales minerales, enzimas y principios inmediatos orgánicos). - B. Citoesqueleto.
Es un entramado tridimensional de fibras de proteinas que se extienden por el citoplasma. Son responsables de:
– Forma celular.
– Movimiento intracelular de los orgánulos.
– Movimiento celular (anclaje de los cilios y flagelos).
– División celular (forma el Huso mitótico). - C. Orgánulos:
- C. 1. Ribosomas:
Son orgánulos no membranosos.
Formados por ARN y proteinas, de forma similar a un grano de café.
Los podemos encontrar unidos a la superficie del retículo endoplasmático rugoso o sueltos en el citoplasma.
Su función es fabricar proteinas. - C. 2. Retículo endoplasmático:
Es un orgánulo membranoso formado por un sistema de túbulos y cisternas interconectados. En él distinguimos dos partes:
1. Retículo endoplasmático rugoso, localizado junto al núcleo, con ribosomas adheridos a la membrana. Interviene en la fabricación, modificación y transporte de proteínas.
2. Retículo endoplasmático liso, es la parte más alejada del núcleo, no tiene ribosomas y en él se sintetizan los lípidos que forman las membranas. - C.3. Aparato de Golgi.
Es un orgánulo membranoso, formado por sáculos aplanados y apilados.
Relacionado con el Retículo endoplasmático.
Recibe las proteinas y los lípidos sintetizados por el RER y el REL, los almacena, los modifica y posteriormente los emite :
Como lisosomas.Como material de reparación de las membranas.Al exterior celular. - C.4. Lisosomas:
Son orgánulos membranosos, formados en el aparato de Golgi, que contienen enzimas digestivos.
Intervienen en el proceso de digestión celular, transformando el alimento capturado por la célula o los estructuras celulares viejas o estropeadas, en moléculas para obtener energía y/o materia prima para los procesos de síntesis celular.
C.5. Peroxisomas.
Son orgánulos membranosos, formados por pequeñas vesículas que contienen enzimas que producen peróxido de hidrógeno (H2O2 agua oxigenada). Su función es neutralizar gran parte de las sustancias tóxicas para la célula. - C.6. Vacuolas.
Orgánulo membranoso, poco numerosas y de gran tamaño en las células vegetales, muy pequeñas en las células animales.
Actúan como almacen de nutrientes o sustancias de desecho y como un regulador de la turgencia/rigidez de la célula. - C.7. Mitocondrias.
Son orgánulos membranosos, limitados por dos membranas: una externa lisa y otra interna que forma pliegues llamados crestas mitocondriales. El espacio interno, la matriz mitocondrial, está ocupado por enzimas.
En las mitocondrias se produce la respiración celular, las moléculas orgánicas se combinan con oxígeno liberando energía en forma de ATP. - C.8. Cloroplastos.
Son un tipo especial de plastos que contienen un pigmento verde llamado clorofila. Es exclusivo de las células vegetales.
Tienen dos membranas, una externa lisa y otra interna con pliegues o tilacoides y el liquido interno llamado estroma.
En los cloroplastos se produce la fotosíntesis, en la que a partir de moléculas inorgánicas y con la energía luminosa se sintetizan moléculas orgánicas. - C.9. Centrosoma.
Es una estructura no membranosa, formada por dos centriolos dispuestos perpendicularmente. Son estructuras tubulares proteicas formadas por nueve grupos de tres microtúbulos, exclusivas de las células animales.
Se encuentran en la base de los cilios y los flagelos y dan lugar al huso mitótico en la división celular.
Núcleo (material genético)
Es un corpúsculo de forma esférica u ovoide, rodeado por una doble membrana que presenta las mismas características que la membrana plasmática. – Contiene el ácido desoxirribonucleico (ADN) que junto a las proteínas y las histonas forma la cromatina (material genético). Durante la fase de mitosis la cromatina se condensa en unas estructuras denominadas cromosomas (las células humanas tienen 46 cromosomas, excepto las células sexuales maduras o gametos). – En su interior contiene el nucléolo, compuesto fundamentalmente por proteínas y ácido ribonucleico (ARN). – Colabora en el almacenamiento, trascripción y transmisión de la información genética.
A menudo resulta útil considerar la célula como una fábrica, analogía que utilizaremos con frecuencia en los capítulos posteriores.
Las membranas envuelven toda la estructura y separan los distintos orgánulos, que pueden considerarse departamentos con funciones especializadas. Así, por ejemplo, el núcleo es la administración central. Contiene, en su DNA, una biblioteca de información para las estructuras y procesos celulares, y emite instrucciones para la regulación adecuada de los negocios de la célula.
Los cloroplastos y las mitocondrias son los generadores de energía (siendo los primeros solares, y los segundos quemadores de combustible).
El citoplasma es el área de trabajo general, en donde la maquinaria proteica (enzimas) lleva a cabo la formación de moléculas nuevas a partir de las materias primas importadas. Los canales moleculares especiales en las membranas entre los compartimientos y entre la célula y su entorno regulan el flujo de moléculas en las direcciones adecuadas.
Al igual que las fábricas, las células tienden a especializarse en su función. Así, por ejemplo, muchas de las células de los organismos superiores están dedicadas en gran parte a la producción y exportación de uno o unos pocos productos moleculares.
Un ligando es un ión o molécula (o grupo funcional) que se une a un átomo metálico central para formar un complejo de coordinación. El enlace entre el metal y el ligando generalmente involucra la donación de uno o más pares de electrones del ligando.
La respuesta celular
Hoy en día sabemos que la respuesta celular a una molécula mensajera, designada en forma general como ligando (hormona, citosina, factortrófico o neurotransmisor), depende de su enlace o interacción con un receptor específico para ese ligando.
Generalmente, el receptor es una proteína que puede estar localizada en la superficie de la célula blanco, el citosol o su núcleo. Las interacciones o uniones ligando-receptor son de alta afinidad, no covalentes, y ocasionan un cambio conformacional en el receptor, el cual inicia una serie de reacciones que conducen a un cambio en la función celular. (caracterizar su especificidad y su cinética de enlace)
Continuamente la membrana está incorporando nuevos componentes (lípidos, proteínas) y retirando otros que ya no se necesitan o estándañados. Por ejemplo, durante el ciclo celular, la membrana duplica su tamaño antes de la división celular.
Receptores (moléculas) localizados en la membrana plasmática (superficie celular)
- Receptores con actividad enzimática.
- Receptores acoplados a proteínas G (Receptores metabotrópicos).
- Receptores sin actividad enzimática, pero asociados a proteínas citosólicas.
- Receptores accesorios o correceptores.
La transmisión de información a nivel celular (interacción estímulo-receptor)
Sobre la función celular: Los virus
- Estructura del virus
La estructura consta de una proteína llamada cápsida y una molécula de ácido nucleico.
Un virus típico consta de una proteína de cubierta protectora, llamada cápsida y una molécula de ácido nucleico (ya sea DNA, ya sea RNA) . La forma de ésta varía desde formas en hélice simple o icosahédricas hasta estructuras más complejas con colas. La cápsida proporciona protección para el genoma del virus frente al ambiente, aunque también participa en el reconocimiento de los receptores, permitiendo que los virus lleguen hasta las células susceptibles del hospedador.
Los virus no son celulares, y se describen, por tanto, como “entidades biológicas” en lugar de como organismos; son parásitos intracelulares que tan sólo pueden crecer invadiendo células.
Dado que los virus no contienen una maquinaria metabólica propia, deben utilizar la de la célula hospedadora para reproducirse.
¿Tiene vida propia el virus?
- Si entendemos como unidad mínima de vida la célula (teoría celular), los virus no son seres vivos.
- Si algo vivo es algo que crece, se reproduce y muere, sí son seres vivos (como las bacterias). Ademas, los virus mutan, lo cual es una propiedad intrínseca de lo vivo.
En virología, se llama “virión” a la forma extracelular del virus, mientras no se encuentra infectando una célula.
En el virión, el material genético se encuentra envuelto por diferentes moléculas que le dan una estructura determinada, llamada “cápside”. Podemos distinguir dos estructuras básicas en la cápside de los viriones, la estructura icosaédrica y la estructura helicoidal, aunque, en ocasiones podemos encontrar viriones con estructuras más complejas.
Por definición, un icosaedro es una figura tridimensional formada por 20 triángulos equiláteros iguales en tamaño. A simple vista, parece caprichoso que algo en la naturaleza sea tan perfecto como puede ser un icosaedro. Sin embargo, la estructura icosaédrica de los virus puede explicarse de forma sencilla: un icosaedro es la figura tridimensional construida a base de un solo monómero que permite el mayor volumen en su interior. Esto es muy beneficioso para los virus que adoptan esta estructura, ya que no necesitan más de un tipo de molécula para formar una cobertura en la que cabe perfectamente su material genético.
En ocasiones podemos encontrar viriones con cubiertas helicoidales. En estos casos, la cubierta protéica de los virus está formada por un único tipo de proteína, dispuesta de forma helicoidal, que deja una cavidad central. En la cavidad central se dispone el material genético del virus.
Al estudiar las condiciones necesarias para la replicación del virus, podemos obtener pruebas sencillas sobre la manera en que actúa la maquinaria celular. Los virus nos proporcionan, pues, ventanas útiles sobre las funciones celulares que ellos comparten durante la infección.
Así, por ejemplo, los virus más pequeños que contienen DNA replican éste utilizando únicamente las enzimas de la célula hospedadora.
Dado su pequeño tamaño, estas moléculas de DNA vírico pueden aislarse y caracterizarse con mucha mayor facilidad que las moléculas de DNA gigantes de los cromosomas celulares.
Los virus de mayor tamaño estimulan la formación de nuevas enzimas tras la infección, y los genes del virus especifican las estructuras de estas enzimas.
Los estudios de estas enzimas han aclarado los mecanismos de regulación genética y han identificado objetivos para el tratamiento de las enfermedades víricas.
Los virus son parásitos intracelulares, básicamente portadores de ácido nucleico y para duplicarse a sí mismos utilizan la maquinaria de reproducción y las fuentes de energía de la célula hospedadora.
A mediados de los años 1980, se empezaron a determinar las estructuras moleculares detalladas de los virus, con lo cual se abrió también la posibilidad del diseño lógico de agentes antivíricos.
Los herbicidas y los pesticidas actúan, en muchos casos, de forma similar, mediante el bloqueo de enzimas o receptores del organismo.
Moléculas biológicas
Las moléculas gigantes o macromoléculas, constituyen una parte importante de la masa de cualquier célula. Por ejemplo, las moléculas de DNA pueden considerarse como “cintas” de las que se extrae linealmente la información genética.
De hecho, las moléculas de DNA de una sola célula humana, si se extendieran de extremo a extremo, alcanzarían una longitud de unos 2 metros.
La síntesis de estas moléculas tan grandes plantea un reto interesante a la célula. Las células utilizan un planteamiento modular para elaborar las moléculas grandes.
La estructura del polímero
Consiste en cadenas principales de átomos de carbono (C), unidos por enlaces covalentes, y estas cadenas están unidas a su vez entre sí por enlaces secundarios o enlaces covalentes (cross-link). Los polímeros forman la mayor parte de la maquinaria estructural y funcional de la célula.
La estructura puede llegar máximo a un 95% de cristalinidad y como mínimo a un 5%. Siempre hay un poco de parte amorfa o cristalina.
Todas estas estructuras DNA son polímeros formados por la unión de unidades prefabricadas o monómeros. La celulosa es un polímero de un azúcar simple, o sacárido, se llama polisacárido.
Dado que la celulosa es un polímero de un azúcar simple, o sacárido, se llama polisacárido.
Este polímero concreto se elabora a partir de unidades monoméricas idénticas, por lo que se denomina homopolímero.
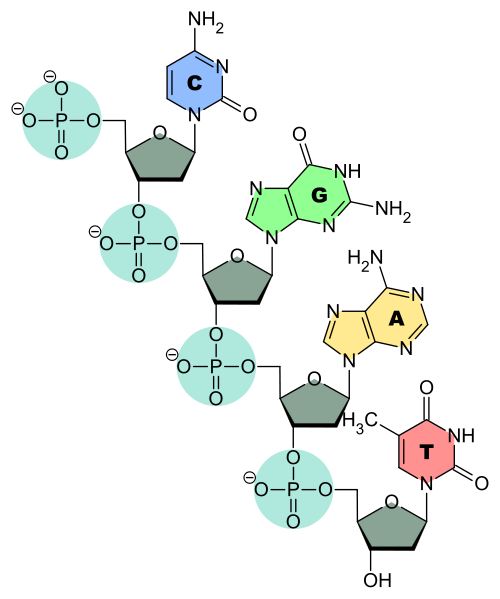
Los ácidos nucleicos son polímeros de cuatro nucleótidos, y por este motivo a los ácidos nucleicos se les denomina también polinucleótidos.
De igual modo, las proteínas se forman mediante las combinaciones de 20 aminoácidos diferentes. Las cadenas proteicas se denominan polipéptidos, término que procede del enlace peptídico que une a dos aminoácidos.
Los ácidos nucleicos, DNA y RNA, participan en el almacenamiento, transmisión y expresión de la información. El DNA o ácido desoxirribonucleico, actúa principalmente como almacén de la información genética, mientras que el RNA o ácido ribonucleico, de estructura similar, interviene en la extracción de la información almacenada en el DNA.
Las proteínas, que tienen una diversidad estructural muy superior a la de los polisacáridos o los ácidos nucleicos, realizan un conjunto más diverso de funciones biológicas.
Otras actúan como sustancias transportadoras, cuyo ejemplo destacado es la hemoglobina, la proteína que transporta oxígeno en la sangre.
Las proteínas pueden transmitir información entre partes distantes de un organismo, como lo hacen las hormonas proteicas y los receptores de la superficie celular que reciben las señales de las hormonas, o pueden defender al organismo frente a la infección, como lo hacen los anticuerpos.
Las más importantes de todas, las proteínas que actúan como enzimas, catalizan las miles de reacciones químicas que se producen en el interior de cada célula.
Los lípidos son un grupo de compuestos químicamente diverso que se clasifican juntos debido a sus estructuras con abundantes hidrocarburos, que les proporcionan una solubilidad muy baja en el medio acuoso de la célula.
Esta baja solubilidad dota a los lípidos para una de sus funciones más importantes, la de actuar como el elemento estructural principal de las membranas que rodean a las células y que las dividen en varios compartimientos.
Capitulo 1
Objetivos de la bioquímica
La bioquímica pretende describir la estructura, la organización y las funciones de la materia viva en términos moleculares.
¿Cuáles son las estructuras químicas de los componentes de la materia viva? ¿De qué forma interactúan estos componentes para dar origen a estructuras supramoleculares organizadas, células, tejidos multicelulares y organismos?
¿Cómo extrae energía de su entorno la materia viva para mantener su existencia? ¿De qué manera almacena y transmite un organismo la información que necesita para crecer y reproducirse de forma exacta?
¿Qué cambios químicos acompañan a la reproducción, el envejecimiento y la muerte de las células y los organismos? ¿Cómo se controlan las reacciones químicas en el interior de las células vivas?
Los bioquímicos se plantean este tipo de preguntas y el estudio de la química de la vida busca las respuestas.
Definición de la Ciencia Bioquímica
El corazón de la bioquímica es la propia naturaleza de la química de la vida.
Aunque solemos describir la bioquímica como una ciencia de la vida y relacionamos sus avances con la historia de la biología, sigue siendo en primer lugar y ante todo una ciencia química.
La bioquímica pretende describir la estructura, la organización y las funciones de la materia viva en términos moleculares. Estudia la química de la vida.
La Bioquímica es el estudio de la base molecular de la vida. (1ª definición)
La bioquímica es una rama de la ciencia que estudia la composición química de los seres vivos, especialmente las proteínas, carbohidratos, lípidos y ácidos nucleicos, además de otras pequeñas moléculas presentes en las células y las reacciones químicas que sufren estos compuestos (metabolismo) que les permiten obtener energía (catabolismo) y generar biomoléculas propias (anabolismo). (2º definición)
Es la ciencia que estudia la base química de las moléculas que componen algunas células y los tejidos, que catalizan las reacciones químicas del metabolismo celular como la digestión, la fotosíntesis y la inmunidad, entre otras muchas cosas. (3º definición)
La bioloqia molecular es una fusión de la bioquímica, la biología celular y la genética.
La distinción entre biología molecular y bioquímica no siempre está clara, puesto que ambas disciplinas toman como campo de actuación la definición completa de la vida en términos moleculares. El término biología molecular se suele utilizar en un sentido más limitado, para indicar el estudio de la estructura y función de los ácidos nucleicos y los aspectos genéticos de la bioquímica, un campo al que podríamos denominar con mayor exactitud genética molecular.
La bioquímica integra el conocimiento de los procesos químicos en células vivas.
Por el contrario la biología molecular concierne principalmente al entendimiento de las interacciones de los diferentes sistemas de la célula, lo que incluye relaciones tales como las que existen entre el ADN y el ARN, la síntesis de proteínas, el metabolismo.
La bioquímica es también una disciplina diferenciada, con su propia identidad. Se distingue por su énfasis en las estructuras y las reacciones de las biomoléculas, en especial las enzimas y la catálisis biológica; por la explicación de las rutas metabólicas y su control; y por el principio de que los procesos vitales pueden comprenderse mediante las leyes de la química.
El objetivo de la ciencia de la bioquímica es explicar la vida en términos moleculares, puesto que actualmente sabemos que no existen diferencias fundamentales entre la materia viva y la que no lo es.
La bioquímica moderna extrae sus conocimientos de la química, la biología celular y la genética, y utiliza técnicas prestadas de la física.
Los descubrimientos que se han realizado en todas estas ciencias han contribuido a impulsar una verdadera biología molecular. Aunque la bioquímica estudia organismos, células y componentes celulares, se trata fundamentalmente de una ciencia química.
Para comprender la influencia de la bioquímica sobre la biología, es preciso conocer los elementos químicos de la materia viva y las estructuras completas de muchos compuestos biológicos (aminoácidos, azúcares, lípidos, nucleótidos, vitaminas y hormonas) y su comportamiento durante las reacciones metabólicas.
Será preciso conocer la estequiometría y los mecanismos de un gran número de reacciones. Además, el conocimiento de los principios básicos de la termodinámica es esencial para entender de qué manera obtienen las plantas la energía de la luz del sol y cómo obtienen los animales la energía de los alimentos.
Las propiedades disolventes del agua son indispensables en los procesos bioquímicos.
Principios de la bioquímica, conceptos y lenguaje. Proceso del descubrimiento en bioquímica.
Organización de los principios de la bioquímica:
- Conformación demostrada por las relaciones entre la estructura tridimensional de las proteínas y su actividad biológica.
- Generación y almacenamiento de la energía metabólica.
- Biosíntesis de los precursores de las macromoléculas.
- Información, almacenamiento, transmisión y expresión de la información genética.
- Fisiología molecular, interacción de la información, conformación y metabolismo en los procesos fisiológicos.
Ramas principales de la bioquímica (ciencia interdisciplinar)
Biología celular (citología)
Es una área de la biología que se dedica al estudio de la morfología y fisiología de las células procariotas y eucariotas. Trata de conocer los orgánulos celulares, su composición bioquímica y su función en el contexto celular tanto en estados fisiológicos como patológicos. Algunas técnicas utilizadas en biología celular tienen que ver con siembra de cultivos celulares, observación por microscopía óptica y electrónica, inmunocitoquímcia, inmunohistoquímica, ELISA o citometría de flujo.
Bioquímica estructural
La bioquímica estructural es una rama de las ciencias de la vida que combina la biología, la física y la química para estudiar los organismos vivos y para resumir algunos principios mutuos que todas las formas de vida comparten.
Química orgánica
Es un área de la química que se encarga del estudio de los compuestos orgánicos, es decir, aquellos que tienen enlaces covalentes carbono-carbono o carbono-hidrógeno. Se trata de una ciencia íntimamente relacionada con la bioquímica, pues en la bioquímica la mayoría de compuestos biológicos participa el carbono.
Química bioorgánica
La química bioorgánica es una disciplina científica de rápido crecimiento que combina la química orgánica y la bioquímica.
Mientras que la bioquímica apunta a la comprensión de los procesos biológicos usando la química, la química bioorgánica intenta expandir las investigaciones orgánico-químicas (es decir, las estructuras, la síntesis y la cinética) hacia la biología. La química bioorgánica es esa rama de la ciencia de la vida que se ocupa del estudio de los procesos biológicos usando métodos químicos.
Enzimología
La enzimología es la rama de la bioquímica que estudia las enzimas, su cinética, estructura y función, así como su relación entre sí.
Bioquímica metabólica
Es la rama de la bioquímica que estudia la generación de energía metabólica en organismos superiores con énfasis en su regulación a nivel molecular, celular y de órganos.También se enfatizan los conceptos y mecanismos químicos de la catálisis enzimática.
Xenobioquímica
La xenobioquímica estudia la conversión metabólica de xenobióticos, especialmente fármacos y contaminantes ambientales. La xenobioquímica explica las causas de las consecuencias farmacológicas y toxicológicas de la presencia de xenobióticos en el organismo vivo.
Inmunología
La inmunología es una rama de la bioquímica que cubre el estudio de los sistemas inmunes en todos los organismos. Fue Mechnikov quien observó por primera vez el fenómeno de la fagocitosis, en el cual el cuerpo se defiende contra un cuerpo extraño y acuñó el término.
La inmunología clasifica, mide y contextualiza:
- Funcionamiento fisiológico del sistema inmunológico en estados tanto de salud como de enfermedades
- Funcionamiento defectuoso del sistema inmune en trastornos inmunológicos
- Características físicas, químicas y fisiológicas de los componentes del sistema inmune in vitro, in situ e in vivo.
La inmunología tiene aplicaciones en numerosas disciplinas de la medicina, particularmente en los campos de trasplante de órganos, oncología, virología, bacteriología, parasitología, psiquiatría y dermatología.
Virología
Area de la biología, que se dedica al estudio de los biosistemas más elementales: los virus. Tanto en su clasificación y reconocimiento, como en su funcionamiento y estructura molecular.
Genética molecular e ingeniería genética
Es un área de la bioquímica y la biología molecular que estudia los genes, su herencia y su expresión. También estudia la inserción de genes, el silenciamiento génico y la expresión diferencial de genes y sus efectos.
Neuroquímica
La neuroquímica es la rama de la bioquímica que estudia los neuroquímicos, incluyendo neurotransmisores y otras moléculas como psicofármacos y neuropéptidos, que influyen en la función de las neuronas.
Este campo dentro de la neurociencia examina cómo neuroquímicos influyen en el funcionamiento de las neuronas, sinapsis y redes neuronales.
Los neuroquímicos analizan la bioquímica y la biología molecular de los compuestos orgánicos en el sistema nervioso y sus funciones en procesos neurales como la plasticidad cortical, la neurogénesis y la diferenciación neural.
Quimiotaxonomía
Merriam-Webster define la quimiotaxonomía como el método de clasificación biológica basado en similitudes en la estructura de ciertos compuestos entre los organismos que se están clasificando.
Ecología química
La ecología química es el estudio de las interacciones entre los organismos y entre los organismos y su entorno, que involucran moléculas o grupos de moléculas específicas denominadas semioquímicas que funcionan como señales para iniciar, modular o terminar una variedad de procesos biológicos.
Unidades de masa y de longitud
La micra : 1 μm = 0,000001 m = 10-6 m ( millonésima de metro ). Se utiliza para medir microorganismos.
El nanómetro : 1 nm = 0,000000001 m = 10-9 m ( mil millonésima de metro). Se utiliza para medir las moléculas de ADN.
El ángstrom : 1 Å = 0,0000000001 m = 10-10 m . Se usa para medir distancias atómicas.
Los modelos moleculares visualizan la estructura tridimensional
La relación entre la estructura tridimensional de las biomoléculas y su función biológica es el motivo de esta introducción.
Utilizaremos tres tipos de modelos atómicos para representar la arquitectura molecular: Los modelos espaciales o modelos compactos, de esferas y varillas, y modelos esqueléticos.
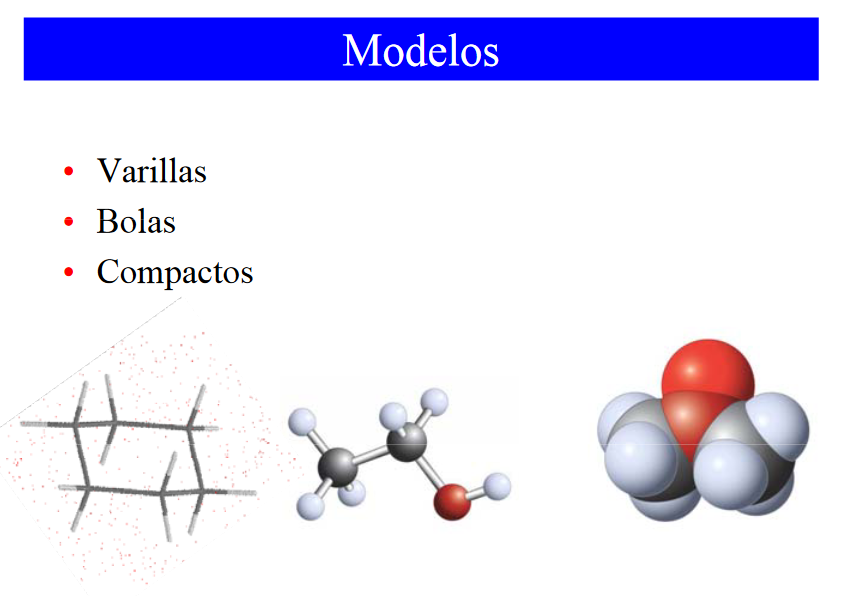
Los modelos espaciales son los más realistas. El tamaño y configuración de un átomo en un modelo espacial viene determinado por sus propiedades de enlace y por los radios de van der Waals.
Recordamos: El Van der Waals radio es igual a la mitad la distancia entre dos átomos no unidas cuando las fuerzas electrostáticas entre ellos son equilibrada. En otras palabras, es la mitad de la distancia más cercana entre dos átomos que no están unidos o dentro de la misma molécula.
Los modelos de esferas y varillas no son tan realistas como los modelos espaciales porque los átomos están representados como esferas con radios más pequeños que los radios de van der Waals. Sin embargo, es más fácil de ver en este modelo la disposición del enlace (varillas). El filamento o conicidad de la varilla indica la dirección del enlace hacia delante o hacia atrás del plano.
Los modelos esqueléticos se utilizan para representar grandes macromoléculas biológicas, tales como moléculas proteicas que tienen varios millares de átomos.
Notación:
- La “p” en frente de un valor, como el pH, pKa y pKb, significa el log del valor después de la “p”.
- El pH es una medida de acidez o alcalinidad de una disolución. El pH indica la concentración de iones de hidrógeno presentes en determinadas disoluciones. La sigla significa potencial de hidrógeno o potencial de hidrogeniones. El significado exacto de la p en «pH» no está claro, pero, de acuerdo con la Fundación Carlsberg, significa «poder de hidrógeno».
- En cambio, pKa es una constante de acidez.
Las interacciones reversibles entre biomoléculas
Química Supramolecular
La Química Supramolecular es la disciplina dentro de la Química que se encarga de estudiar el autoensamblaje supramolecular, “la Química más allá de la molécula”. (def 1)
La Química Supramolecular se dedica al estudio, diseño y síntesis de estructuras moleculares unidas entre sí mediante enlaces no covalentes; por ello también ha sido denominada “química más allá de la molécula”, “química del enlace no covalente” o bien “química no molecular”. (def 2)
El término supramolecular fue introducido en el año 1978 por J.-M. Lehn para hacer referencia a los conjuntos ordenados de moléculas que se mantienen unidas por una variedad de interacciones de naturaleza no covalente.
Coloquialmente, se utilizan otras expresiones para referirse a la Química Supramolecular, como “la química del enlace no covalente” o “la química del ensamblaje molecular y las fuerzas intermoleculares”. De cualquier modo, todas las expresiones mencionan el carácter no covalente de las interacciones que se establecen para dar lugar a las estructuras supramoleculares. Las estructuras supramoleculares son entidades complejas formadas por la asociación de dos o más especies enlazadas a través de fuerzas débiles.
En el proceso de formación de una supramolécula toman parte una molécula que actúa como anfitriona (host) y otra como huésped (guest), que se une a la primera para dar lugar a un complejo anfitrión-huésped. Comúnmente, el anfitrión es una molécula grande o un agregado, como un enzima o un compuesto cíclico, con una cavidad central de tamaño adecuado. El huésped puede ser un ión inorgánico sencillo o bien una molécula más compleja, como una hormona o un neurotransmisor. Las asociaciones entre las moléculas anfitrión y huésped se basan en interacciones intermoleculares que son, en general, más débiles que los enlaces covalentes.
El principio de la complejación multisitio es muy habitual en sistemas biológicos, asegurando la eficiencia de la replicación, de las interacciones enzima-sustrato o antígeno-anticuerpo, así como otras funciones biológicas importantes.
Un requerimiento importante para la combinación multisitio es la complementariedad entre los lugares de complejación de las moléculas anfitrión y huésped, ya que la complejación es más eficiente cuanto mejor encajan entre ellas. Este es el principio general de llave-cerradura (key-lock) propuesto por E. Fisher.
Los primeros estudios en el campo de la Química Supramolecular se centraron en el atrapamiento selectivo de cationes alcalinos por parte de ligandos macrocíclicos y macropolicíclicos naturales o sintéticos, como los éteres corona y los criptandos. Este hecho condujo al nacimiento del reconocimiento molecular como un nuevo dominio de la investigación química que se expandió y recibió el nombre de Química Supramolecular.
Cabe distinguir adecuadamente los términos supramolécula y supermolécula. La palabra supramolecular es un término de significado más amplio, que concierne a todas las ramas de la Química que presentan asociaciones polimoleculares más o menos organizadas. Por otra parte, en Química Teórica, el procedimiento computacional que trata las asociaciones moleculares de igual manera que si fuesen una sola entidad descrita por una única función de onda, se denomina aproximación supermolecular.
Interacciones Intermoleculares
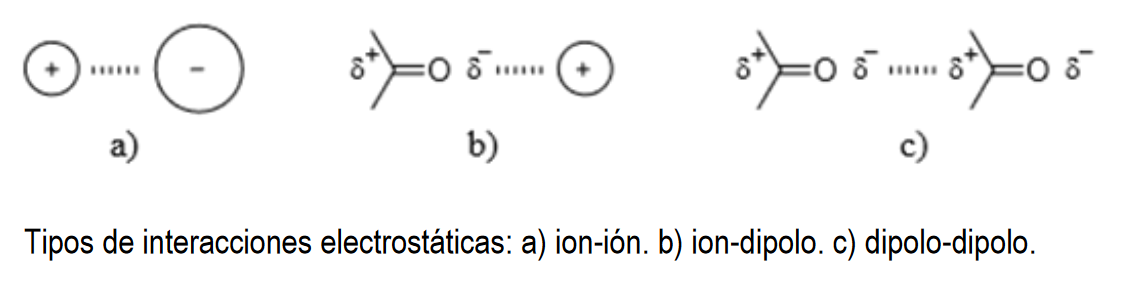
Fuerzas inductivas
Los efectos inductivos surgen de la distorsión de una molécula provocada por el campo eléctrico que generan las moléculas vecinas. En una interacción entre una molécula dipolar y otra apolar, el campo eléctrico de la molécula polar distorsiona la distribución de carga electrónica de la molécula que no lo es, produciendo en ella un momento dipolar inducido.
Puesto que la energía de inducción es fruto de la distorsión de la distribución de carga como respuesta a un campo externo, es siempre negativa para las moléculas en sus estados electrónicos fundamentales; y no es aditiva porque la interacción entre dos moléculas se ve afectada por la presencia de terceras.
La polarizabilidad molecular es la tendencia de una molécula a ser polarizada, es decir, la facilidad con que se crea en ella un momento dipolar inducido a causa de campos eléctricos externos producidos, por ejemplo, por moléculas vecinas.
La polarizabilidad en los átomos y moléculas se define de acuerdo con la fuerza que adquiere el momento dipolar inducido en el campo eléctrico, siendo una constante de proporcionalidad entre el campo externo y el momento inducido en la molécula no polar.
La polarizabilidad molecular es un tensor que puede representarse como una matriz 3×3 simétrica, de manera que posee únicamente seis componentes independientes.
Fuerzas dispersivas
F. London las describió usando la teoría perturbacional de segundo orden, apuntando una relación entre dichas fuerzas y la dispersión óptica en gases, denominándolas fuerzas de dispersión.
También son denominadas fuerzas de London y son las únicas de largo alcance presentes en todas las interacciones moleculares. Constituyen la contribución más importante a las fuerzas de van der Waals, excepto en moléculas polares pequeñas, y el único término de la energía de largo alcance en el caso de la interacción de dos moléculas neutras apolares.
Enlace de Hidrógeno
Teoría de Lewis
Ácido: “Sustancia que contiene al menos un átomo capaz de aceptar un par de electrones y formar un enlace covalente coordinado”.
Base: “Sustancia que contiene al menos un átomo capaz de aportar un par de electrones para formar un enlace covalente coordinado”.
Tipos de geometrías en la formación de enlaces de hidrógeno:
- Lineal; girado; bifurcado en el dador; bifurcado en el aceptor; trifurcado; bifurcado en dos centros.
